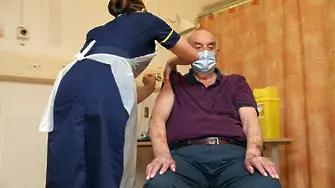
Наличните понастоящем данни от клинични изпитвания не позволяват оценка на ефикасността на ваксината при лица над 55 години.
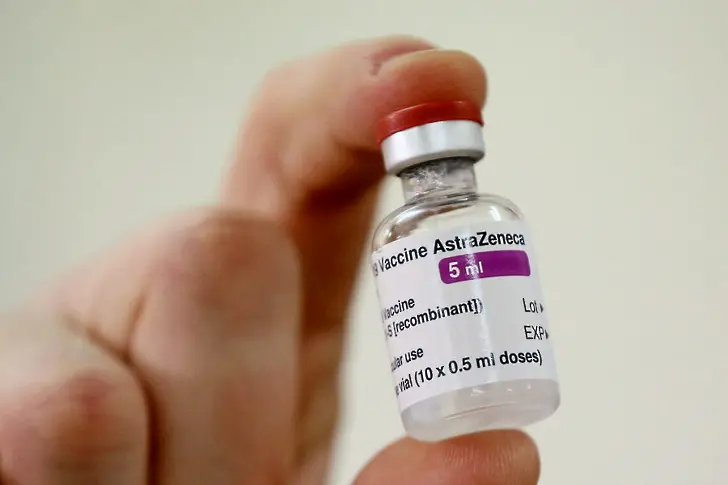
Това пише в Кратката характеристика на ваксината на "АстраЗенека", която в петък получи одобрение за употреба в ЕС. Днес Министерството на здравеопазването публикува на български език освен характеристиката на продукта, също и листовката му от Европейската агенция по лекарствата/European Medicines agency (EMA).
Ваксината на "АстраЗенека" е с 60% ефикасност, се посочва в документа с подробна информация за продукта:
"Резултатите показват 59,5% намаление на симптоматичните случаи на COVID-19 при хора, на които е приложена ваксината (64 от 5 258 са развили COVID-19 с проявени симптоми)".
В указанията за употреба се посочва, че ваксината е за лица на възраст между 18 и повече години. Уточнява се, че наличните данни не позволяват оценка при лица над 55 години, както и за ефикасността, безопасността и имуногенността при имунокопрометирани хора, включително и пациенти на имуносупресивна терапия.
Има ограничен опит при бременни жени. Липсват данни за хора под 18 г.
Постигането изцяло на защитата се очаква да стане на около 15-ия ден след втората доза.
Ето някои от характеристиките на продукта, от който България е заявила общо 4,5 млн. дози:
Имунизирането с ваксината на "АстраЗенека" е за лица на възраст 18 и повече години.
Курсът на ваксинaция се състои от две отделни дози по 0,5 ml всяка. Втората доза трябва да се приложи между 4 и 12 седмици (28 до 84 дни) след първата.
Безопасността и ефикасността при деца и юноши (по-малки от 18 години) все още не са установени. Липсват данни.
Ваксинацията трябва да се отложи при лица, страдащи от остро тежко фебрилно заболяване или остра инфекция. Наличието на лека инфекция и/или слабо повишена температура обаче не трябва да забавя ваксинацията.
Както при други интрамускулни инжекции, ваксината трябва да се прилага с повишено внимание при лица получаващи антикоагулантна терапия или такива с тромбоцитопения или някакво нарушение на кръвосъсирването (например хемофилия) тъй като при тези лица може да се появи кървене или образуване на синини след интрамускулно приложение.
Имунокомпрометирани лица
Ефикасността, безопасността и имуногенността на ваксината не са оценени при имунокомпрометирани лица, включително такива, получаващи имуносупресивна терапия.
Ефикасността на COVID-19 Vaccine AstraZeneca може да бъде по-ниска при имуносупресирани лица.
Продължителност на защитата
Продължителността на осигурената от ваксината защита е неизвестна, тъй като тя се установява във все още продължаващи клинични изпитвания.
Ограничения на ефективността на ваксината
Защитата започва приблизително 3 седмици след първата доза. Лицата може да не са напълно защитени до 15-ия ден след приложение на втората доза. Както при всички ваксини, имунизацията може да не осигури защита на всички лица.
Наличните понастоящем данни от клинични изпитвания не позволяват оценка на ефикасността на ваксината при лица над 55 години.
Нежелани лекарствени реакции
Резюме на профила на безопасност
Общата безопасност на ваксината се основава на междинен анализ на сборни данни от четири клинични изпитвания, проведени в Обединеното кралство, Бразилия и Южна Африка. По време на анализа 23 745 участници на възраст ≥18 години са рандомизирани и са получили или COVID-19 Vaccine AstraZeneca, или контрола. От тях 12 021 са получили най-малко една доза, а 8266 - две дози. Средната продължителност на проследяване е 62 дни след доза 2.
Най-често съобщаваните нежелани реакции са:
чувствителност на мястото на инжектиране (63,7%),
болка на мястото на инжектиране (54,2%)
главоболие (52,6%)
умора (53,1%)
миалгия (44,0%)
неразположение (44,2%)
пирексия (включва усещане за повишена температура (33,6%) иповишена температура >38°C (7,9%))
втрисане (31,9%)
артралгия (26,4%)
гадене (21,9%).
Повечето нежелани реакции са леки до умерени по тежест и обикновено отзвучават в рамките на няколко дни след ваксинацията. В сравнение с първата доза нежеланите реакции, съобщени след втората доза, са по-леки и се съобщават по-рядко.
Реактогенността обикновено е била по-лека и се съобщава по-рядко при възрастни в по-напреднала възраст (≥65 години).
Профилът на безопасност е съвместим сред участниците с или без предходни данни за SARS-CoV-2 инфекция на изходно ниво; броят на серопозитивните участници на изходно ниво е 718 (3,0%).
Данните показват, че защитата, започва приблизително 3 седмици след първата доза на ваксината и се запазва до 12 седмици. Втора доза трябва да се приложи в интервал от 4 до 12 седмици след първата доза.
Популация в старческа възраст
Сред участниците на възраст между 56 и 65 години, 8 случая на COVID-19 са съобщени при тези получаващи COVID-19 Vaccine AstraZeneca (≥15 дни след доза 2) сравнено с 9 случая в контролата; 2 и 6 случая с COVID-19 са съобщени при участници на възраст 65 години, съответно с COVID-19 Vaccine AstraZeneca (≥15 дни след доза 2) и контролата.