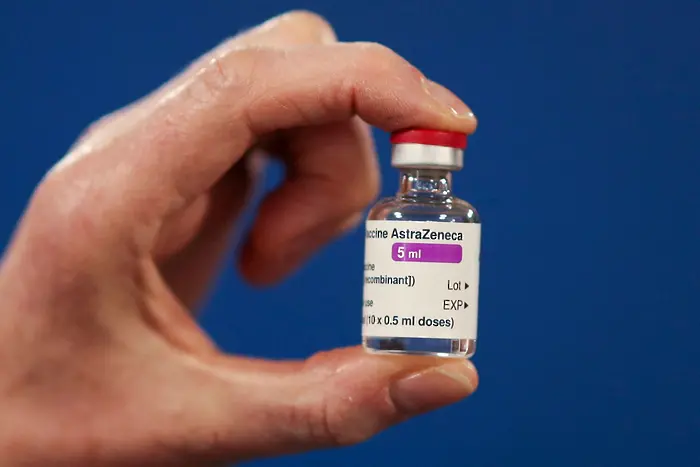
Европейската агенция по лекарствата (ЕАЛ) съобщи днес, че е приела молба за оторизация на коронавирусната ваксина, разработена от Оксфордския университет и от британско-шведката фармацевтична група AstraZeneca, която вече се прилага в Обединеното кралство.
Агенцията ще разгледа молбата по ускорена процедура, се казва в съобщението на уебсайта ѝ.
Мнение за пазарната оторизация би могло да бъде издадено до 29 януари, се казва още в съобщението.
Толкова кратка времева рамка за оценката е възможна, само защото ЕАЛ вече е разгледала някои данни за ваксината по време на текущ преглед. В тази фаза, ЕАЛ е оценила данните от лабораторните изследвания (неклинични данни), от качеството на ваксината (за съставките и начина, по който се произвежда) и някои доказателства за безопасността и ефикасността ѝ от междинните анализи по време на клиничните изпитания в Обединеното кралство, Бразилия и Южна Африка.
Компанията е предоставила допълнителна информация по въпроси, свързани с качеството, безопасността и ефикасността, която агенцията разглежда в момента.
Досега Европейският съюз е одобрил и неговите държави членки вече използват ваксините на Pfizer-BIONtech (германско-американска) и на Moderna (американска). И двете са разработени възоснова на информационна рибонуклеинова киселина (РНК).
Ваксината на Oxford-AstraZeneca е генетично модифициран вирус на обикновена настинка у шимпанзета. Той е променен, за да не причинява инфекция при хората и носи част от строежа на коронавируса, известна като "протеин на шипа", с който вирусът се закрепва за клетките в човешкия организъм. Имунната система на пациента разпознава този протеин като заплаха и се опитва да го унищожи, като произвежда антитела. Когато тя влезе в контакт с истински вирус, вече "знае" какво да прави.
Ваксината на Oxford-AstraZeneca беше втората ваксина, одобрена в Обединеното кралство, след като ваксината Pfizer-BioNTech получи зелена светлина през декември.
Британската ваксина е значително по-евтина от двете американски и е лесна за масово производство. От решаващо значение е, че може да се съхранява в стандартен хладилник - за разлика от тази на Pfizer-BioNTech, която се нуждае от ултра студено съхранение при -70 градуса Целзий и на тази на Moderna, която изисква температура от -20 Целзий.