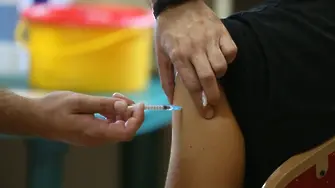
Европейският лекарственият регулатор реши днес, че поставянето на подсилваща доза на ваксината „Спайквакс“ срещу COVID-19 на компанията „Модерна“ може да се препоръча за хора на възраст от 18 години нагоре.
До това заключение е стигнала Комисията по лекарствени продукти за човешка употреба към Европейската агенция по лекарствата (ЕАЛ).
Решението е в резултат на получени данни, според които трета доза „Спайквакс“ може да се поставя 6 до 8 месеца след втората. Изследванията установили, че втората доза води до повишаване на нивото на антитела у пълнолетни, у които това ниво отслабва.
Подсилващата доза се състои от половината от първата, използвана при ваксинирането.
Данните показват, че ефектите при подсилващата доза за подобни на тези при втората. Рисковете от възпалително състояние на сърцето или други много редки странични ефекти след подсилване продължават да бъдат следени много внимателно.
На национално ниво здравните власти могат да издадат официална препоръка за използването на подсилващи дози, като вземат предвид местната епидемиологична ситуация, данните за ефекта и ограничените данни за безопасността на тази доза.
Досега трета доза можеше да се слага само от ваксината на "Пфайзер".
Европейската лекарствена агенция обяви пак днес и че ще започне ускорено изследване на лекарството срещу ковид на американската лаборатория "Мерк".
Ако бъде одобрено от регулатора, лекарството на "Мерк" може да окаже значително влияние върху хода на борбата с коронавирусната пандемия.
"Комисията за лекарства за употреба от хора на ЕАЛ започна изследване на антивирусния медикамент за орална употреба молнупиравир (. . .), разработен от "Мерк" (. . .) за лечението на COVID-19 при пълнолетни", съобщи базираният в Амстердам европейски лекарствен регулатор.
Предварителните резултати от лабораторното изследване и клиничните изпитания сочат, че медикаментът е в състояние да намалява способността на коронавируса да се множи в човешкото тяло, като по този начин се възпрепятства необходимостта от приемане в болница и леталният изход, уточнява ЕАЛ.
Ако бъде одобрено, се очаква лекарството да допринесе сериозно за предотвратяване на тежките форми на COVID.